
多重核酸检测是感染性疾病诊断、肿瘤标志物分析和空间组学研究的重要基础。然而,传统荧光多重检测往往依赖多种颜色、复杂光谱拆分和精细校准。通道越多,串色、背景干扰和解码误差也越容易累积。 有没有可能只用一种荧光颜色,借助空间位置同时解析多个核酸靶标?北京化工大学苏昕团队给出了一个新的答案:不再把靶标信息“塞进颜色”,而是把它们写入微球的空间位置中。 |
研究亮点:让“位置”成为新的荧光通道 日前,北京化工大学生命学院苏昕、王诗卉团队在 Nature Communications 发表题为“Spatial fluorescence barcode by transiently luminescent DNA beads”的研究论文。该研究提出了一种基于瞬时发光DNA微球(transiently luminescent DNA beads, TLDBs)的空间荧光条形码(spatial fluorescence barcode, SFB)策略,为高通量、低串扰、可复用的核酸多重检测提供了新方案。 该系统的核心思想可以概括为“单色读出、空间编码、酶促复位”。研究团队将Y形DNA探针固定在链霉亲和素包被的聚苯乙烯微球表面。当目标核酸出现时,靶标通过链置换反应移除猝灭链,使微球表面的Cy5荧光短暂亮起;随后,体系中的核酸酶降解已结合的靶标,使猝灭链重新杂交,微球回到暗态并进入下一轮检测。 通过顺序引入不同靶标并记录微球发光位置,系统可以建立单色空间荧光条形码码本(mSFBC)。在未知样本检测中,只需将发光微球的位置与码本进行空间共定位比对,即可识别样本中包含哪些核酸靶标。 |
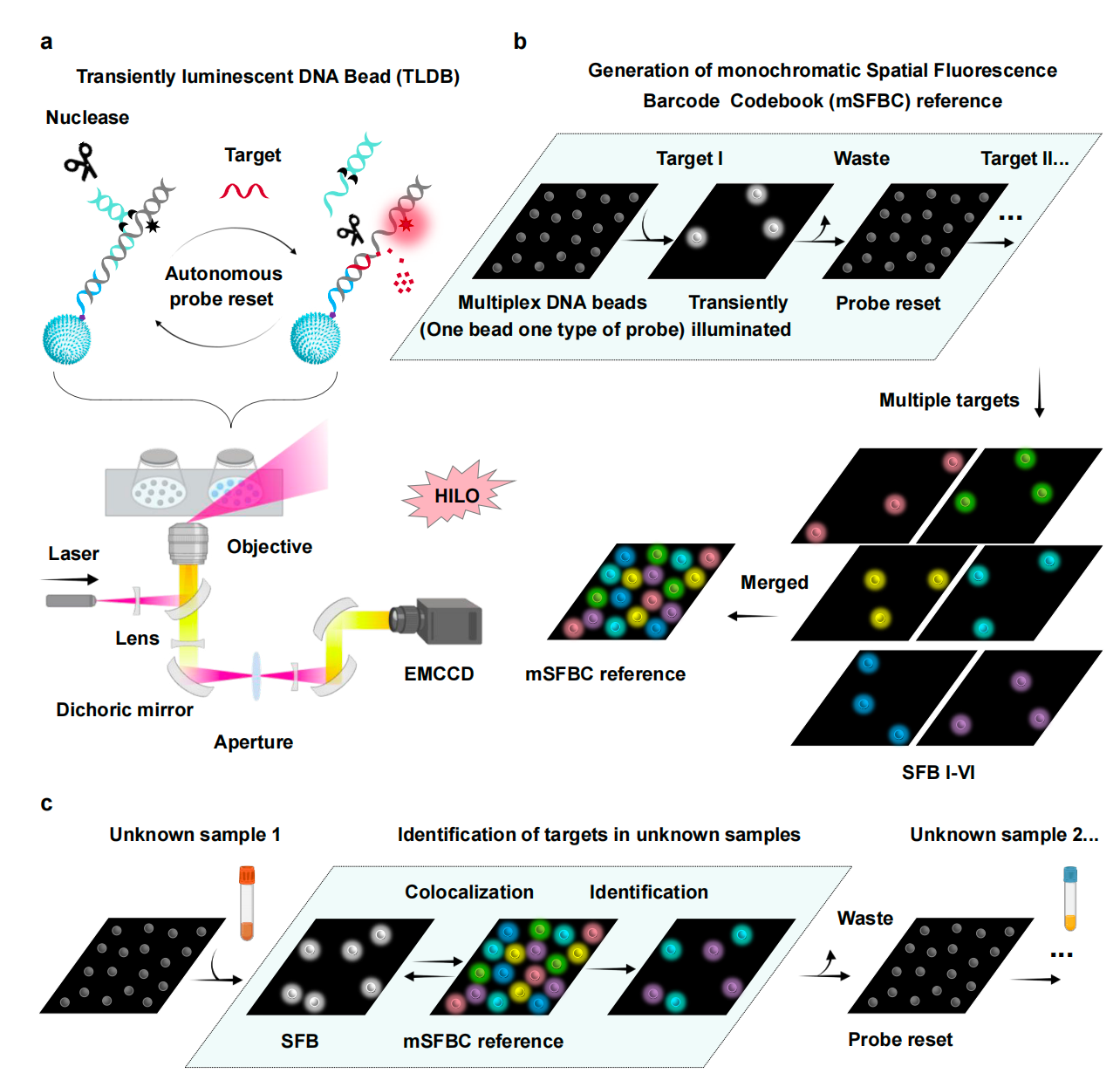
图1:单色空间荧光条形码(SFB)系统的工作流程和原理。
从原理验证到临床样本:空间条形码的可用性 围绕“准确编码、循环复用、真实样本检测”三个关键问题,团队系统验证了SFB平台的性能。结果显示,七种DNA微球仅在匹配靶标存在时产生明确荧光响应,非匹配组合几乎无交叉反应,证明了该体系良好的正交性。Y形探针可经历多轮“激活—复位”循环,微球空间位置在连续检测后仍保持稳定;在DNA模型靶标检测中,平台检测限约为1 pM。 在应用验证中,团队将SFB用于临床相关病原体标志基因检测,覆盖多种重要病原体的物种特异性和高毒力相关基因。临床感染血液样本检测结果与参考测序结果一致,并可在同一码本下实现多样本批量分析。进一步地,团队将核酸酶模块由ExoIII替换为RNase H,实现乳腺癌组织中多种miRNA标志物的同步识别,展示了SFB在病原体检测和肿瘤标志物分析中的应用潜力。 |
“让荧光只负责发光,让空间负责解码。” SFB策略将分子识别、动态DNA反应、酶促复位和显微空间定位整合在同一平台中,为未来低成本、可扩展的多重核酸检测提供了新的技术路线。 |
论文链接:https://doi.org/10.1038/s41467-025-67410-3 |
图片:田丹丹
文稿:田丹丹
审核:贾广联 王兴 曹辉
