我校苏昕副教授与密西根大学Alexander Johnson-Buck博士合作,利用DNA聚合酶(DNAP)合作开发了一种以DNA为模板的“计时钟”探针,以时间标签来标记物种,实现多重性检测。这些探针利用等温DNAP介导的延伸信号的时间延迟来区分相应靶标,利用DNAP对核苷酸的持续装载能力及其动力学的可控性,可以使用单一荧光基团在均质溶液中实现多重病原体DNA检测。这一成果近期发表在Nano Letters上,我校博士研究生邓莹楠为文章第一作者,苏昕副教授和Alexander Johnson-Buck博士为共同通讯作者。
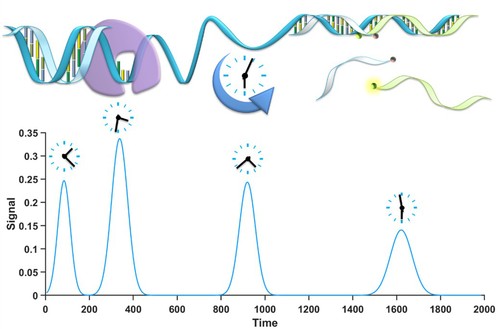
 图1. 用于多重检测的DNA计时钟探针与模拟信号示意图
图1. 用于多重检测的DNA计时钟探针与模拟信号示意图
新型冠状病毒的爆发给人类敲响了警钟。多重病原体快速分子检测是应对病毒大爆发的必要手段。目前,多重检测主要依赖多种颜色的荧光分子标记。但是,按颜色划分的信号类型非常有限,且同时分析多种荧光基团会产生由于光谱之间相互串扰而导致特异性差等问题。

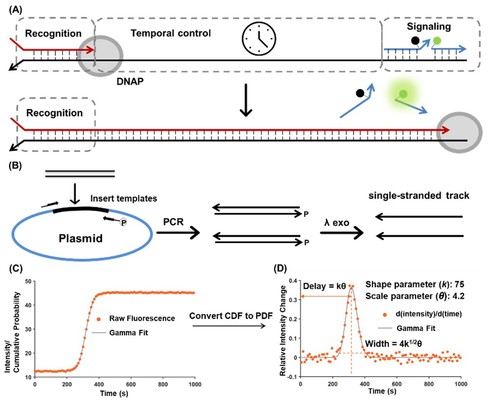
图2. DNA计时钟探针的设计原理、信号响应及理论模拟
针对上述挑战,作者设计了基于DNA计时钟的多重核酸检测系统,使用称为“聚合酶跑道”的DNAP底物的长度来控制信号产生的时间。通过DNAP的底物长度依赖的时间延迟,可以使其在预定的时间下得到荧光信号的爆发。待检测的靶标物质作为DNAP的引物,通过聚合过程发生链置换反应产生荧光信号的上升(图2A)。为不同的靶标匹配不同长度的“聚合酶跑道”,则相当于给不同的靶标标记可分辨的时间信号标签。通过理论建模,作者发现这一信号产生的过程符合伽马分布,为信号拟合和条件优化提供了依据(图2C)。
作者通过优化聚合酶种类、浓度、温度、dNTP及一价阳离子浓度优化了两个靶标检测的分辨率,并且引入色谱分析中常用的分辨率参数(R)呈现优化结果。在此基础上,作者利用单一荧光在均相溶液中实现了多重病原体基因组DNA的同时检测(图3)。由于任何仪器的荧光检测阈值范围有限,若同时多个DNA计时钟探针的连续荧光恢复的信号积累最终可能会限制多重靶标的数量。因此,希望在单次信号产生后便立即消除其荧光信号。作者使用引入接收DNA链及氧化石墨烯材料两种方法使得荧光信号达到单次振荡的效果,实现类似“色谱峰”一样的荧光-时间信号(图4)。

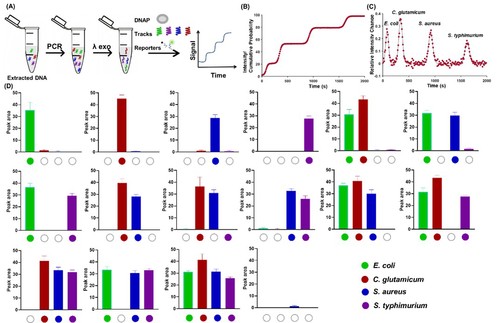
图3. 病原体基因组DNA的多重检测。
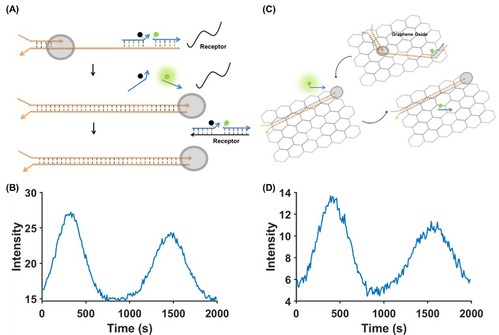
 图4. 具有震荡信号的DNA计时钟探针
图4. 具有震荡信号的DNA计时钟探针
这一方法实现了在均相溶液中,利用单一荧光一次性检测多重病原体,将在病毒检测、分子诊断、多重成像、DNA纳米技术等领域有广泛应用。
论文链接:https://pubs.acs.org/doi/10.1021/acs.nanolett.0c00313
苏昕副教授,北京化工大学博士生导师,北京化工大学青年百人计划入选者。2010年于南开大学获得学士学位,2015年于北京大学获得博士学位,2013-2015年在美国密歇根大学做访问学者。2015年加入北京化工大学,从事生物医学工程-纳米技术-生物安全交叉研究,主要方向包括:单分子荧光分析、核酸纳米技术、合成基因电路、纳米机器人、体外诊断等。目前主持国家自然科学基金面上项目、国家重点研发计划子课题、北京市优秀人才项目以及其他国家级项目。
